








氧分子在制备大分子以及同大分子反应中可起多种作用.
(1)氧是一种强的自由基捕捉剂,因为氧本身是双自由基:
R·+·O—O· → R—O—O· (23-1)
反应(23-1)表明氧对自由基聚合起阻聚剂或缓聚剂的作用.过氧自由基虽然是稳定的,但并不是惰性的.
(2)在适当的条件下过氧自由基同单体结合形成可增长的自由基:
R—O—O·+M → R—O—O—M· (23-2)
在此氧起到如同共聚单体的作用.
(3)在氧存在下有时观察到聚合速率增加,所以,氧也被归为引发剂.
(4)无论是氧分子或过氧自由基都可进行抽氢反应;这类反应导致醇酸树脂交联和有关聚合物的氧化降解.
(5)最后,氧在催化剂影响下可使某些含有活泼氢的化合物如酚类进行聚合,但是,由于酚氧自由基的稳定性如反应(23-3)所示,所以酚类化合物也是最普通的一类抗氧剂.
在后一领域早期的工作者证明2,6-二烷基4-卤代苯酚在铁氰化钾的影响下氧化偶联生成聚合物.这反应所生成的聚合物具有类似于由2,4,6-三卤代苯酚的银盐生成的聚合物的性质
这反应被认为是按自由基的历程进行的.只有带有氧化物基团的芳环也带有卤素取代基时,酚-醚二聚体才能聚合;根据此事实,设想在这反应中的主要反应基团是酚氧自由基.
1958年,海(Hay)和他的同事们用2,6-二烷基酚类化合物或某些乙炔衍生物与氧分子在亚铜盐-胺催化下反应,可形成高分子量线形聚合物:
这反应可在室温下顺利进行,并明显地具有逐步缩合反应的特征.
关于二烷基酚类聚合的一些有趣现象是很值得注意的.虽然氧处于不同的相中,但从反应来看是在均相中进行的.这种反常现象可用铜-胺络合物是一活泼的氧化剂来解释;而氧的唯一作用是维持铜为二价状态.其次,当烷基取代苯酚的2、6位而不是3、5位时,而且2、6位上的取代基体积是较小的(像甲基),则聚醚的形成就很顺利进行.当烷基体积增大时,将发生与C—O偶联相竞争的C—C偶联反应,导致形成联苯醌:
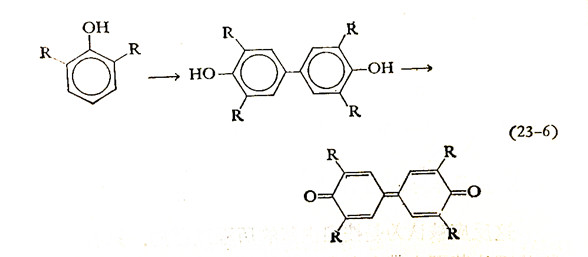
关于促进C—O或C—C偶联因素的研究表明:
(1)酚或铜离子浓度以及溶剂的介电常数对偶联速率均没有明显影响;
(2)增加吡啶对铜的比例可降低C—C偶联,当吡啶/铜的克分子比大于10时则完全排除了C—C偶联;而用双配位基胺如N,N,N',N'—四甲基乙二胺则在当量比为2比1时发生突变;
(3)无论增加反应温度或增加取代基体积或用空间阻碍大的配位体(2,6-二甲基吡啶或喹啉)*都可以增加C—C偶联的量.
作者们解释这种现象是由于有两种不同配位数的铜-胺络合物:
Cu(吡啶)m+n吡啶 → Cu(吡啶)m+n (23-7)
具有较低配位数的络合物有利于C—C偶联,而具有较高配位数的络合物则有利于C—O偶联.在吡啶-甲醇介质中所作进一步机理的研究对于了解催化剂性质是有帮助的.
因为,无论是增加苯酚上或配位体上取代基的体积都将妨碍聚合,所以海和恩德雷斯(Endres)研究了改变配位体上取代基的体积对邻甲苯酚聚合的影响.邻甲苯酚是可以进行邻位偶联的,他们用空间阻碍大的配位体2,6-二甲基吡啶得到了支化的聚合物.
基本的增长过程与自由基转移历程及紧接着两个自由基进行偶联的历程有关.
活泼的酚氧自由基X也可以其共振式烯丙基型的自由基Y存在.两个Y偶联产生联苯醌;X和Y的偶联得到如下产物:
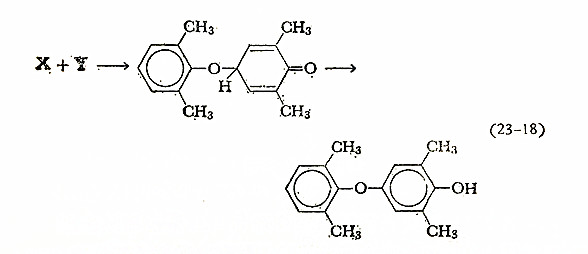
这些自由基在整个过程中可能不是游离的,而是络合存在的.或在它们的反应过程中有一步或几步是受金属-配位体络合物(Cu:N≡)所决定的.
在生长过程中也可能存在交换反应,使自由基-偶联历程成为真正的逐步生长过程.
反应(23-8)中涉及由Cu(Ⅰ)氧化成Cu(Ⅱ),接着形成络合物A.在吡啶/铜低比率(1:1)时反应按途径Ⅰ进行,酚氧离子置换甲氧基而形成络合物B.络合物B进行氧化还原反应[反应(23-10)]生成3,3',5,5'-四甲基-4,4'二羟基联苯和Cu(Ⅰ)的络合物.因为Cu(Ⅰ)的络合物跟氧和2,6-二甲基苯
酚反应再生成络合物B[反应(23-11)],使这反应连续下去.同时,双酚通过反应(23-12)被氧化成四甲基联苯醌.这反应在100℃时是可逆的,用单体可再生联苯二酚.
在吡啶/铜高比率时(10:1),反应按途径(Ⅱ)进行,络合物A跟吡啶反应生成络合物C,络合物C再通过复分解形成络合物D[反应(23-14)].络合物D的自动氧化还原反应导致聚合物的形成,同时铜被还原.这反应如途径(Ⅰ)通过Cu(Ⅰ)氧化成Cu(Ⅱ)并再生成络合物D[反应(23-16)],使其继续进行下去.最近海改进了由阻碍酚如2,6-二苯基苯酚形成聚合物的方法.
* 配位体/Cu高比率的影响似乎不如配位体空间效应的影响大,但生成的速率是较慢的.