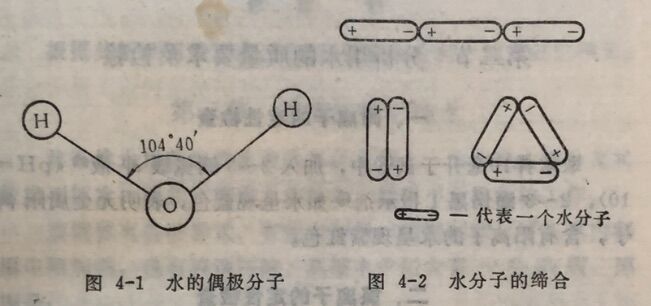
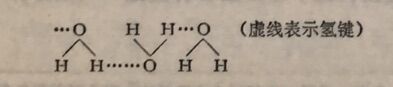氢键的键能一般在数千卡/摩尔。由于水分子间有氢键,使分子间产生较强的结合力,由简单的分子H₂O结合成较复杂的分子(H₂O)ₓ, 但又不引起水的化学性质改变的现象叫水分子的缔合(图4-2)。
水在液态时是缔合的,在3. 98°C时以(H₂O),存在,故密度最大。气态时水以单分子存在,使水汽化还要克服氢键力,因此水的沸点比分子量相近而分子间没有氢键的化合物的沸点高。同样原因,使水的温度升高也要消耗能量使缔合的分子破坏,因而水的比热大。温度较高的水洗物品易洗干净也是由于水中缔合的分子受到破坏,容易把脏物洗下来。
水只有微弱的导电性,水按下式发生自偶电离。
H₂O+H₂O⇔H₃O⁺+OH⁻
可简写成 H₂O⇔H⁺+OH⁻
精确实验测得25°C纯水中的离子浓度是:
(H⁺)=1.0×10⁻⁷M
(OH⁻)=1.0×10⁻⁷M
水的电离度随温度升高而增大。
25°C时,纯水的理论电导率为5.5× 10⁻⁸西/厘米(s/cm) 换算成电阻率是18.2x10⁶欧姆·厘米(Ω.cm) (注:电导的单位西门子相当于来制的1/欧姆或姆欧)如果水中有了电解质,它的电导率将增加。测定水的电导率可以反映水中存在电解质的多少。但是要注意此法测不出非导电物质的污染。当纯水接触空气以后,空气中的二氧化碳落于水,使其电导率增加,可达1x10⁶西/厘米,二氧化碳易用加热法除去,不影响使用。
水是很容易起化学反应的物质,它能和许多金属氧化物及非金属氧化物化合,和最活泼的金属(如钠等)反应放出氢,水也参与很多化学反应。
























![水杨酸甲酯[冬青油]](images/201812/thumb_img/964_thumb_G_1545823931913.jpg)