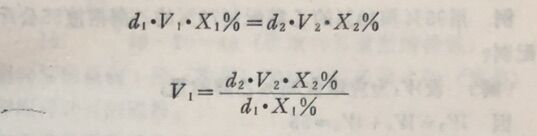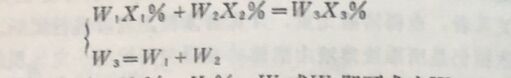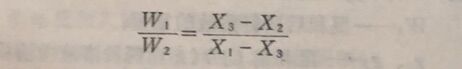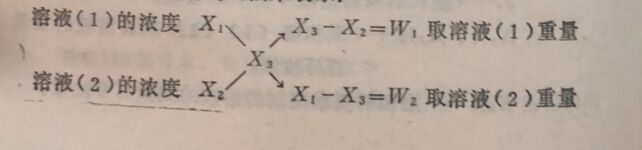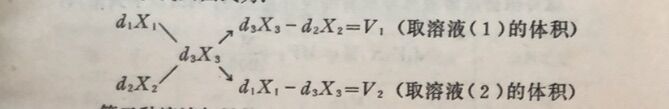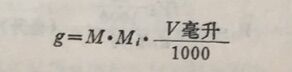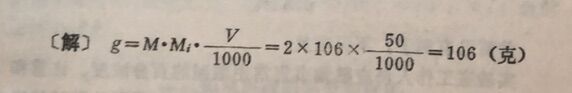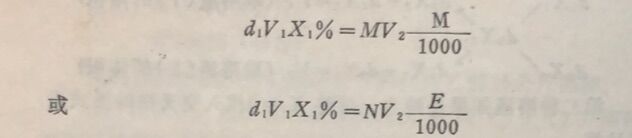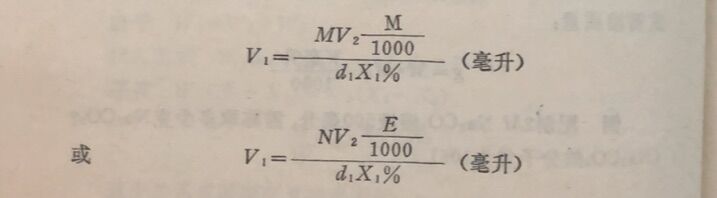一般溶液的配制
铜臭 / 2022-07-06
1.以重量百分浓度表示的溶液的配制
(1) 用固体溶质配制百分浓度溶液 根据重量百分浓度的定义,在托盘天平上(对于称样量小于0.1克的固体可以在物理天平或分析天平上称,读出2位有效数字即可)称取溶质x克(x=W·X%),所用溶质重量应为W-x克,如以水为溶质,一般近似认为水的比重为1,用量简量取W- x毫升体积的水,将溶质加入其中,完全溶解即可。
例 配制10% KI的溶液200克,如何配制?
[解]称取Kl x=200×10% = 20(克)
取溶剂水 200 - 20=180 (克)
量取180毫升水,将KI溶解于水中。
(2)用较浓的液体试剂配制较稀的溶液由 于浓溶液的取用量以量取体积较为方便,故一般需查阅酸、碱溶液的浓度-比重关系表,查得溶液比重,计算出体积,然后进行配制。计算的依据仍是所取浓溶液中溶质的重量和所配的一定体积的溶液中溶质的重量相等。
例 配制10% (比重1.08) KOH溶液1000毫升,需要40% 比重1.41的KOH溶液多少毫升?
V₁=1.08×1000×10%/1.41×40%=191(毫升)
其它定义的百分浓度溶液的配制所需溶质和溶剂的量也可根据浓度定义推导出来。
(3)两种不同百分浓度的溶液混合配制所需浓度的溶液这类问题计算的依据仍是两种已知浓度溶液中所含溶质重量之和等于配制后溶液中溶质的重量。
①计算法: 用求解未知数的方法计算。
设W₁、W₂—混和前(1) (2)两种溶液的重量;
W₃一混和后所得溶液的重量;
g₁、g₂混和前 (1)(2)两种溶液中溶质的重量;
g₃混和后所得溶液中溶质的重量;
X₁%、X₂%—混和前 (1) (2)两种溶液的重量百分浓度;
X₃%—混和后 要求配制的溶液的重量百分浓度。
列出等式
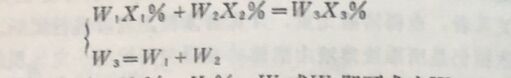
已知X₁%、X₂%、X₃%、W₃或W₂即可求出W₁。
例 用95%和40%的 乙醇配制70%的乙醇溶液55公斤,如何配制?
[解] 设W₁为应取含95%乙醇的量;
因 W₃=W₁+ W₂=55
有 W₂=55-W₁
列出等式 95W₁+ 40(55 - W)=55x70
求出 W₁=30 (公斤)
W₂=25 (公斤)
配制方法为取95%乙醇30公斤和40%乙醇25公斤混和。
②交叉法:此法是找出混和时所取的(1) (2)两种溶液的重量比或体积比。由于混和前后溶液中溶质的重量相等,所以
W₁X₁% +W₂X₂% =W₃X₃%
等式两端乘100 W₁X₁+W₂X₂=W₃X₃
由于 W₃=W₁+ W₂
代入上式 W₁X₁+W₂X₂=W₁X₃+W₂X₃
移项 W₁(X₁- X₃)=W₂(X₃-X₂)
这个关系式可用交叉法来表示:
例 怎样用60%和10%两种硫酸来配制20%的H₂SO₄溶液?

用60%的硫酸1份(重量)和10%的硫酸4份(重量)相混和即配得20%的硫酸。
如欲求出所取溶液的体积,必须在重量百分浓度上乘以比重再交叉。交叉图式为:
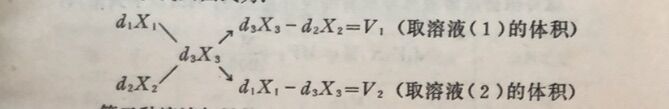
第二种溶液如果是纯水,可将X₂=0代入交叉法的图式进行计算。
2.以体积摩尔浓度和当量浓度表示的溶液的配制
(1)溶质为固体的溶液的配制方法根 据浓度的定义,计算出所需溶质的克数。设所需溶质量为g,配制体积摩尔浓度需溶质量:
例 配制2M Na₂CO₃溶液500毫升,需称取多少克Na₂CO₃?(Na₂CO₃的分子量为106)
配制当量浓度溶液需溶质量:
g=N·E·V(毫升)/1000
例配制2N Na₂CO₃溶液500毫升,需称取多少克Na₂CO₃(Na₂CO₃的当量为53)
[解]g=N·E·V/1000=2×53×500/1000=53(克)
(2)用市售浓溶液配制稀溶液的方法根 据前面介绍的方法把浓溶液的浓度由重量百分浓度换算为当量浓度,再根据稀释规则进行配制。
也可根据浓溶液稀释前后溶质的量相等,列出以下关系式:
式中 V2—需配制的溶液的体积;
V₁ —取比重d₁,浓度X₁的溶液的体积。
从上二式求出需取浓溶液的体积:
前面已有例子,不再重复。
实验室工作人员应熟知市售常用酸碱的百分浓度、比重和其摩尔浓度、当量浓度。表5-4列出了几个最重要的酸碱的浓度,供配制溶液时使用。其余的可查阅本书附录。
3.比例浓度溶液的配制
例 欲配制1:2HCl溶液150毫升, 如何配制?
[解]设取浓HClx毫升,用水量应为2x毫升,据比例浓度定义,有
x +2x=150 x=50 (毫升)
配制方法为量取水100毫升于烧杯中, 加入浓HCI 50毫升,混匀即可。
表 5-4 一些商品试剂的近似比重、百分含量和摩尔浓度、当量浓度表
| 名称 |
重量百分浓度 |
比重 |
摩尔浓度 |
当量浓度 |
| 盐酸 |
36~38%
|
1.18 |
12 |
12 |
| 硫酸 |
95~98%
|
1.84 |
18 |
36 |
|
|
|
|
(全部H+被中和) |
| 硝酸 |
65~68%
|
1.52 |
16 |
16 |
| 磷酸 |
85%
|
1.71 |
15 |
45 |
|
|
|
|
(全部H+被中和) |
| 氢氟酸 |
42%
|
1.15 |
24 |
24 |
| 高氯酸 |
70~72%
|
1.75 |
12 |
12 |
| 乙酸 |
99%
|
1.05 |
18 |
18 |
| 氨水 |
25~28%(NH₃)
|
0.90 |
14 |
14 |
有的分析操作规程直接给出试剂配制方法,但其浓度表示 方法并不和我们所介绍的一致,百分浓度,有时指明把定 量的溶质溶于100毫升水中,它不属于w/W、w/V、v/V表示的百分浓度。