第七副族的通性
铜臭 / 2022-08-09
一、第七副族的通性
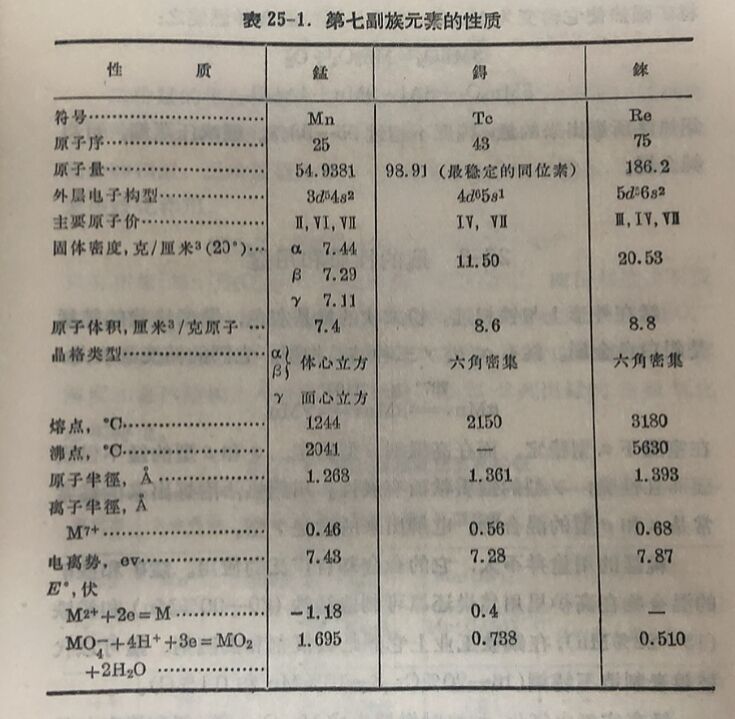
表25-1汇列錳副族元素的重要特性常数。本副族各元素原 子的外电层(n-1)d, ns电子数为7,开始成对,渐趋稳定,故本副族各元素随着原子序的增加,电离势仍继模递增, 熔点、沸点等也随着升高(錸的沸点达最高)。在本副族内各項性质皆依Mn-Re大序递变,不过鍀和錸的原子半徑比較相近,其他性质也較相似,而与錳的差別較大。它們皆可表现为+1至+7不同的价态,但高价的稳定性是随着原子量的增加而增高。錳以Mn⁺⁺为最稳定,七价的MnO₄⁻为强氧化剂,这由下列电偶电位可見:
MnO₄⁻+8H⁺+5e=Mn⁺⁺+4H₂O E⁰=151伏
二价的鍀和錸只在少数絡合物中稳定,簡单的离子不存在。鍀的重要化合物皆呈IV和VI态,III、IV和VI态的化合物皆很难制得。錸的V和VI态的化合物不易制备,III、IV和VI态为常見。这三个金属在平常温度对非金属元素皆不活泼,在較高湿度时可与大多数非金属反应。
二、錳的存在和冶炼
錳的主要矿石是軟錳矿MnO₂·nH₂O,其他尚有黑錳矿Mn₂O,水锰矿MnO(OH)以及褐锰矿Mn₂O₃。
冶炼錳现在最常用是鋁热法。因鋁与软锰矿作用剧烈,故先将矿强热使它轉变为Mn₂O然后与鋁粉混合井燃烧之:
3MnO₂=Mn₃O₄+O₂
3Mn₂O₄+8Al=9Mn+4Al₂O₃
鋁热法所炼出来的錳,炖度不超过95-98%。 程减玉蒸闻,可得炖金属。
三、錳的性质和用途
錳在外形上与铁相近。粉末状的錳是灰色,紧密块状的越锰是銀白色金局。錳有α、β、γ三种结晶构型。它們的轉变温度是:
在室温下α型稳定,而在高温則β型稳定。α和β型的錳不但质 硬而且性脆; γ型的錳质軟而有展性。 用鋁热法冶炼出来的錳常常是α和β型的混合物。电解出来的錳是γ型。
純錳的用途并不大,它的合金却有广泛的应用。錳矿和铁矿 的混合物在高炉里用焦炭还原可制造錳铁(60-90%Mn)和鉍铁 (15-22%Mn),在鋼铁工业上它們是去氧剂和去硫剂。錳可以代 替鎳来制造不銹鋼(16-20%Cr、8-10%Mn和0.1%C)。
錳在空气中氧化,加热时燃燒生成Mn₃O₄。氟、氯和溴在加热时与錳直接作用。氦在1200°以上与錳化合形成氮化物Mn₃N₂, 反应甚至比鎂还快。熔融的錳溶解碳后形成碳化物Mn₃C (与铁 相似)。錳与硫共热时可形成MnS。錳不与氩作用。Mn-Mn⁺⁺电偶的电极电位远在氢之上,因此,它很容易溶于稀酸,形成Mn⁺⁺离子而釋出氫:
Mn+2H⁺=Mn⁺⁺+Hg
也溶于瀼硫酸而放出SO₂,溶于硝酸,放出NO。