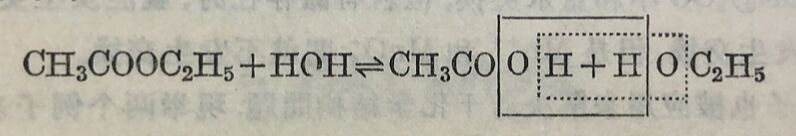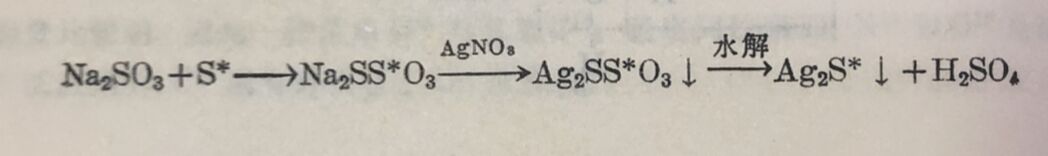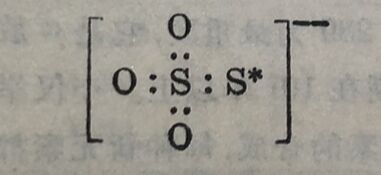标記原子
铜臭 / 2022-08-12
物质在变化过程中究竟經过了什么步驟和途徑,在三十年前是个不容易回答的問题。譬如說,水在人体中究竞停留多少时候?\这一問题的解决,必须使歙入的水和人体中原有的水有所区 别;但是必须仍然是水。同位素恰好能够浦足这一要求。 如果饮入稀的孤水,例如既1%D₂O的水,只要檢驗在什么时候排出的尿中沒有重水。这段时問就代表着水在人体内停留的时間。实驗秸果确定它是两星期。在这个实驗中,氘就演扮着标記原子的角色。因为它比氢較重,可以从水的密度加以精密测定。以上是使用稳定同位素的一个例子。标記原子有着显示踪迹的作用,因此也叫做示踪原子。
利用放射性同位素作为标記原子,更为便利,因为放射性的测量比較灵敏而方便。用放射性磷作为标記原子,可做实驗得出结論:磷在骨骼中停留的时間是1个月。
标記原子的应用范圉是多种多样的,例如研究化学反应历程、化学结构、键的极性、分析化学、扩散現象等等时,都可应用标記原子。下面在介紹常用的标記原子之后,仅将举出一些典型的例子来說明标記原子的用途。
1.常用的同位素
这里列示了一些常用的标記原子,包括稳定同位索和放射性同位素两个部分。
原则上,尽可能使用放射性同位素,因为如上所述,放射性容易测定,例如用計数管(本章1节)就可很方便地测量共放射性。但是,象氮和氧的放 射性同位素,半衰期太短,(最长寿命的氮放射性同位案N¹³的牛衰期是 10.05 分;而最长寿命的氧放射性同位案O¹⁵的半衰期是118秒)都不合用, 因此必须用N¹⁵和O¹⁸。其次, 放射性氫同位素T的β能最很弱,較难测定,同时D便宜得多,因此一般都用D,而不用T。C¹³也比較便宜,但是C¹⁴的β⁻能量比较弱,因此般常用 C¹³而不用C¹⁴。稳定同位素D、N¹⁵和O¹⁸是被广泛应用的,C¹³则有时代替了Cu的应用。
表27-10 放射性同位素举例
| 原子序 |
同位素 |
射线 |
半衰期 |
制法(仅举一例) |
|
1
6
9
11
15
16
17
26
27
53
|
T³
C¹⁴
F¹⁸
Na²²
P³²
S³⁵
Cl³⁸
Fe⁵⁹
Co⁶⁰
I¹²⁸
|
β⁻
β⁻
β⁺
β⁺,γ
β⁻
β⁻
β⁻
β⁻,γ
β⁻,γ
β⁻,γ
|
12.46年
5720年
1.87小时
2.6年
14.50天
87.1天
37.27分
47.1天
4.95年
24.99分
|
Be⁹(n,α)
N¹⁴(n,p)
F¹⁹(n,2n)
Na²³(n,2n)
Si³²(n,p)
S³⁴(n,p)
K⁴⁰(n,α)
Fe⁵⁸(n,γ)
Co⁵⁹(n,γ)
I¹²⁷(n,γ)
|
2. 同位素在研究化学反应历程中的应用
同位素作为标記原子,在解决化学反应历程的問题中起着不可替代的作用。下面举出两个例子加以证明。
(i)酯化反应 在下列酯化和水解的可逆反应中:
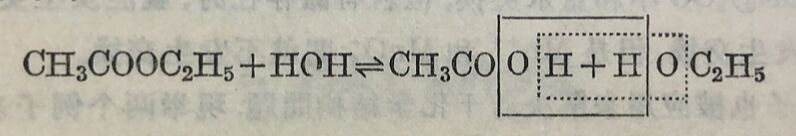
究竟是酸基的羥和醇基的氨结合为水呢(在上式中用实錢标明)?还是酸基的氢和醇基的羥结为水呢(在上式中用虚裁标明)?如果不用标記原子,这一問題是无法解容的。普萊义(Polanyi)于1934年用O¹⁸水作为标記原子,即用 H₂O¹⁸来水解酯,发现O¹⁸仅进入酸中,而不进入醇中,这就证明了第一种历程(实线框)是实际进行的,也就是說,酸基的羥和醇基的氫相互作用而成为水:
CH₃COOC₂H₅+HO¹⁸H⇔CH₂COO¹⁸H+HOC₂H₅
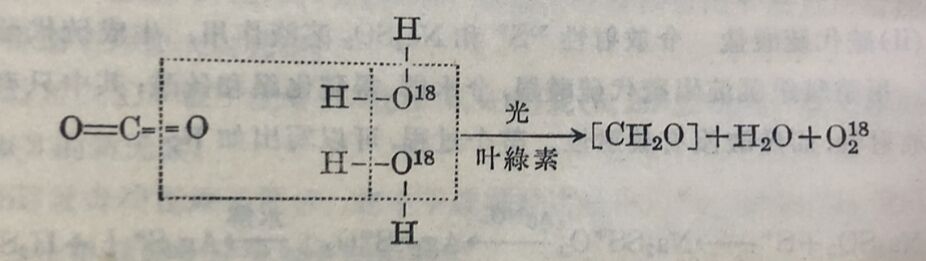
(ii)植物光合作用在植物的光合作用中, 用O¹⁸证明一分子二氧化碳是和两分子水作用的:
这个结论,是根据了所用的重氧水H₂O¹⁸中的O¹⁸全部进入氧分子中。假使是象先前所假定的一个CO₂分子和一个H₂O分子相作用,那末只能有一串的O¹⁸原子进入氧分子,这是和实验结果相矛盾的。
3. 同位素交換和化学结构
重氨与水問不发生交换(除非有接触剂存在),而水和重水間就即立刻发生交换,这是和键的极性有关。强极性的鍵容易断开,并发生交换,例如
C₂H₅OH+D₂O=C₂H₅OD+HDO
有的强极性键本身已有电离存在,例如醋酸,当然容易和重水交换:
CH₃COOH+D₂O=CH₂COOD+HDO
除—OH基中的丑外,-NHI基中的H也能立刘发生交换:
NH₃+3D₂O=ND₃+3HDO
卤化氢中的H也能立刻发生交换。反之,象甲基或乙基中的氨就不发生交换。
丙酮(CH₃)₂CO不和重水交换,但若有碱存在时,就能发生交换。Mn⁺⁺和Mn³⁺間发生交换,但是Mn³⁺和MnO₄⁻問就不发生交换。
标記原子也被应用来解决若干化学结构問题,現举两个例子来作既明。
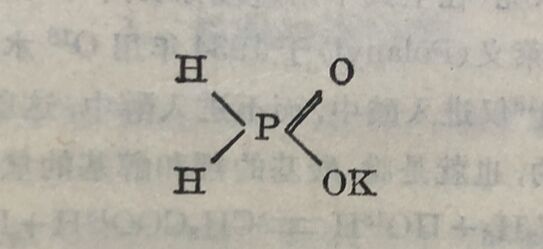
(i)次磷酸盐KH₂PO₂由于和D₂O沒有交换,就证明了它具有下列结构:
就是两个氩原子是和磷以共价键直接联结的。如果有羥基(一OH)存在, 那末其中的H就能立刻和D₂O中的D发生交换了。
(ii)碗代硫酸盐 令放射性³⁵S*和Na₂SO₃溶液作用,生成硫代硫酸根离子。用硝酸銀沉淀出硫代硫酸銀,令水解,得硫化銀和硫酸;其中只有硫化銀有放射生,而硫酸没有放射性。整个过程,可以写出如下:
由此证明在硫代硫酸根結构中,两个硫原子是处于不同地位的,并且它們之間沒有交換。如果两个硫原子在結构中地位相同,或两者之間发生交换,那末产物硫酸中也应当有一半的放射性。上述硫代硫酸根离子的結构如下: