液相色谱实验的方法
抖化学 / 2022-10-04
液相色谱实验的方法:所用设备包括Waters 6000输液泵,流动相由装有干燥管的玻璃贮液槽供应。进样系统是一个Valco高压进样阀,或者一个Varian注样系统,设计成可用皮下注射器在高压下操作。采用的儿根柱全部用淤浆充填技术[6]装填以Partisil 10。对于高度保留的溶质使用100毫米柱,4.6毫米内径,对于中等的或弱保留的溶质使用250毫米柱,4. 6毫米内径。柱温用水套管控制恒温于25±0.5℃。检测器用LDC UV 254纤米监控器,或LDC折光计检测器,其选择取决于所检测溶质的消光系数或折光指数。检测器出口直接连接一个25毫升或50毫升的A级滴定管,这样可以测量绝对保留体积。采用的流速范围在1到3毫升/分之间,测量强保留溶质的保留体积时用高流速以节省展开时间。所用样品的体积范围是2到10微升,溶质的浓度调节到与所使用的检测系统灵敏度相适应的范围。所有溶剂均经通过活化的硅胶仔细地使之干燥,各种溶剂混合物是以重量或体积为基础配制的,即称取已知量的溶剂放人500毫升容量瓶中,加分散溶剂(常用庚烷)到刻度。进行任何测定之前,先用30~35倍于柱死体积的溶剂通过系统以保证平衡。所有保留时间的测量均进行两次,如两次的误差在士0.5%之内,就取其平均值。如超出了0.5%,则重复第三次,取相差不超过0.5%的两次平均值作为保留体积。
图3-3不同溶质校正保留体积的倒数对正庚烷中极性溶剂%W/V的曲线。色谱柱,250×4.6毫米内径; 充填剂,Partisil103溶质: A,苯甲醇; B, 3-苯基-1-丙醇; C,脱氧皮质甾酮醇。极性溶剂: A,四氢呋喃; B,四氢呋哺; C,异丙醇
3-2-1 1/V'=A+Bcp关系式的验证(式中Cp是极性溶剂在分散介质中的浓度)
选择了两种极性溶剂,四氢呋哺和异丙醇;所用溶质是苯甲醇,1-苯基-3-丙醇和脱氧皮质甾酮醇。分散介质是庚烷,展开溶质所用流动相分别为庚烷中含8到30%W/V的四氢呋喃和16到76%的异丙醇。每种流动相对三种溶质都使用了一系列的浓度。所得结果综合示于表3-1, 1/V' 对Cp的关系曲线则示于图3-3。
可以看到函数1/V'=A+Bcp的相关关系由所测定的指数值得到完全的确证。溶质脱氧皮质甾酮醇用异丙醇/庚烷混合溶液展开的结果表明直到高达90%W/V的流动相组成仍维持有这一关系。
3-2-2极性溶质在庚烷中为低浓度时对函数1/V'=A+Bcp的检验
前已指出[4\5]由于硅胶没有完全钝化,在极性溶剂的浓度超过1或2%W/V之前,低浓度的极性溶剂在非极性分散介质中的行为极为不同。因此,在硅胶进行钝化的溶剂浓度范围内考察方程(3-2)给出的函数的变化将是很有意思的。
用几种极性溶剂分散于庚烷的溶液,对一系列不同溶质进行色谱展开。.溶液的浓度范围从大约0.2%到7.0% W/V。所用的溶质和溶剂有:
|
溶质
|
溶剂 |
| 苯基甲基甲醇 |
异丙醇 |
| 菲 |
氯仿 |
| 苯甲醇 |
乙酸乙酯 |
| 苯基甲基甲醇 |
乙酸乙酯 |
| 硝基苯 |
氯仿 |
用庚烷中含有各种浓度的极性溶剂,测定了各个溶质的保留体积。所得结果示于图3-4。
可看到在极性溶剂浓度不足以使硅胶钝化的情况下,1/V'与极性溶剂浓度之间的线性关系被打破了。也可看到,对于一些相对低保留值的溶质一即与两个相的作用力为同一数量级一当极性溶剂的浓度减低时,吸附剂的活化引起保留体积迅速增大,这
种增大发生于极性溶剂在庚烷中的浓度大约处于0.8到1.2%w/V之间。再者,当中等极性的溶剂氯仿,其浓度大约为1 .3% W/V氯仿/庚烷时,吸附剂对于保留值较低的溶质来说就完全钝化了。这与Snydert]的意见相反,他设想中等极性溶剂必须在高浓度才能将吸附剂完全钝化。
但如果溶质是强烈保留的,即溶质和吸附剂之间的作用力明显地大于溶质和溶剂间力,则吸附剂在低浓度极性溶剂中的活化,.对溶质的保留只有较小的作用。但可看到庚烷中的极性溶剂浓度在3到4%之间时曲线就偏离直线,而当溶剂浓度减低时,
保留值的增加速度变得稍小些。从而可以一般地说,由溶剂极性减少而致的吸附剂钝化,将促使在he'值小于5左右时流出溶质的保留值迅速增大。反之,对于已经充分保留的溶质,当吸附剂活化时,其保留值变化很小,而且这对低极性和高极性的流动相都是正确的。
3-2-3 用单一溶质对不同的极性溶剂检验函数1/V'=4+Bcp
使用标准的、填充以Partisil10的250毫米×4.6毫米内径柱,测定了溶质苯基甲基甲醇的校正保留体积,流动相为庚烷中含一系列浓度的下列溶剂:
| 异丙醇 |
四氢呋喃 |
| 正丁醇 |
乙酸甲酯 |
| 正戊醇 |
乙酸乙酯 |
| 二恶烷 |
乙酸丙酯 |
乙酸丁酯
在这些条件下,由于采用同一溶质,不同溶剂之间的保留值变化将反映溶剂在溶质一溶剂相互作用方面的影响。
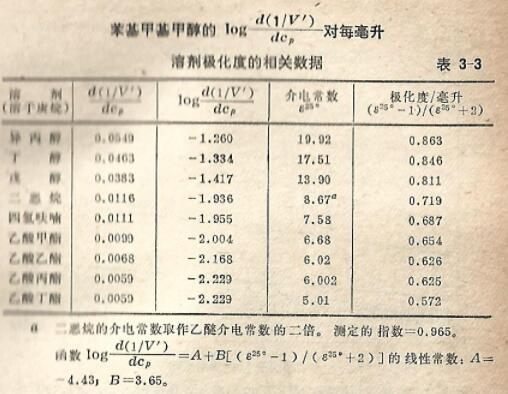
所得结果示于表3-2,1/V '对以极性溶剂在庚烷中的%W/V表示的流动相组成的关系曲线则示于图3-5。可看到对于所有溶剂均得到出色的相关性,并由表3-2的测定指数所确证。从图3-5得知,以曲线斜率表示的溶质与流动相的相互作用,似乎与所有
极性溶剂的所谓极性有关。曾尝试将表3-2给出的斜率与极性溶剂的不同物理参数相连系。表3-3给出了由介电常数值「δ]用简单的公式(δ-1)/(δ+2)计算得的每毫升的极化度,以及图36中曲线的斜率及共对数。
将斜率的对数和溶剂的极化度值作图,使符合于线性函数y=A+B㏄根据这一关系得到的结果也列于表3-3。斜率的对数与溶剂极化度的关系曲线则示于图3-6。
可以看出得到了良好的相关关系,但应指出,二恶烷的每毫升极化度不是直接得自介电常数。二恶烷中两个偶极是反向的,因此相互抵消,所提供的介电常数并不反映溶质一溶剂相互作用方面溶剂的极性。这是采用系统的整体特性来描述分子效应的又
一个不利的例子。因而将二恶烷的介电常数值取作乙醚的二倍。采用了这一数值后,可看到二恶烷的位置接近通过其它溶剂极化值的回归曲线。由此可知溶剂一溶质相互作用对保留值的影响似乎是与每毫升极化度的指数成比例的,从而可表示如下式:
Aexp(ap)=Aexp{a[(δ-1)/(δ+2)]}
式中P是单位体积溶剂的极化度;δ是在25℃测定的溶剂介电常数;A和a是常数。
a 二恶烷的介也常数取作乙醚介电常数的二倍。测定的指数=0.965。
d(1/V')
函数log-------------------=A+B[ (δ25°-1)/(δ25°+2) ]的线性常数: A=4.43;B=3.65。
dCp
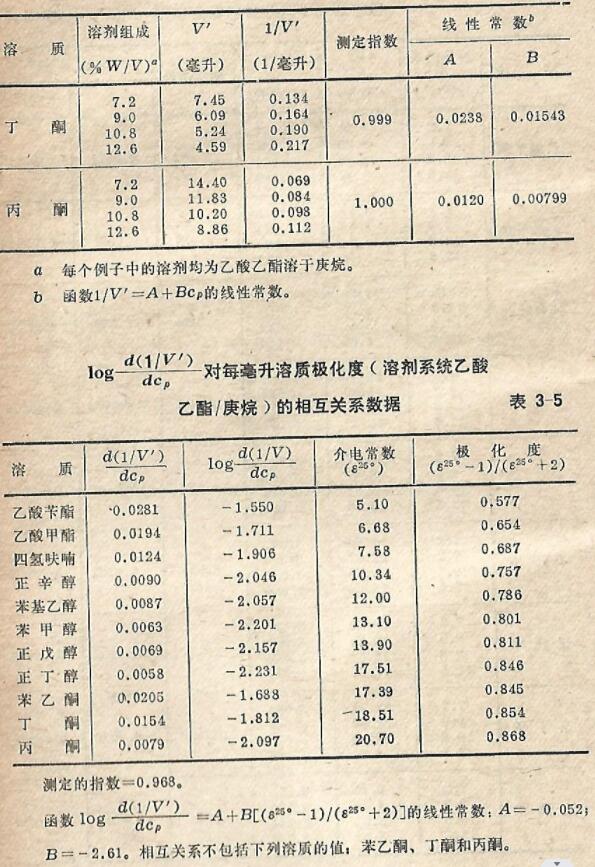
3-2-4用同一极性溶剂在庚烷中的一系列浓度对不同的溶质检验函数1/V'=A+Bc,用一根标准的250毫米,4.6毫米内径柱,充填以Partisil10,测定了表3-4所列溶质的校正保留体积,所用流动相是庚烷中含有7.2到12.6% w/V浓度范围的乙酸乙酯。在应用同一
极性溶剂的条件下,保留体积与极性溶剂浓度之间的关系,将为乙酸乙酯与不同溶质之间相互作用力的函数。所得结果列于表3-4, 1/V'与流动相组成的关系曲线示于图3-7。可看到对于所有的溶质再次得到极好的相关关系,并为表3-4中测定的指数所确证。似于使用不同极性溶剂实验的结果,溶质与乙酸乙酯之间相互作用的差异,似乎与溶质的极性有关。
表3-5将根据各溶质介电常数计算的每毫升极化度[8]和图3-7中曲线的斜率及其对数-一并列出。将斜率的对数和相应的溶剂极化度值作图,使符合于线性方程y=A+B㏄,根据这一相互关系,所得的结果列于表3-5及图3-8。其中对于含有酯、醚和醇基的溶质可获得很好的相关关系,但带有酮基部分的溶质则偏离其它溶质的同归曲线相当一段距离。于是,溶质的相互作用也可用表达式Be”P描述之,共中P是溶质的单位体积极化度,B和β是常数。酮类的反常行为原因不很肯定,但可能是酮类在硅胶的酸性表面易手发生烯醇化,而这种烯醇化作用可能受乙酸乙酯在流动相中的浓度所制约。根据曲线可知酮类的色谱行为似乎处于醚和醇之间。这点是可以预期的,但由介电常数推导得的每毫升极化度指出,它们的行为应更类似于醇类。因此,对于酮类溶质的反常行为的另-解释是,在测量介电常数时,由于 外加电场的结果,所测得的数值反映了酮的烯醇特性,而不是酮的特性。
32-5以同一极性溶剂乙酸乙酯与不同分散介质混合作为流动相对不同的溶质检验函数1/V'=A+ Bcp
采川标准的250毫米,4.6毫米内径柱,充填以Partisil 10,用含乙酸乙酯4.51% w/V的不同烃类化合物测定了下列溶质的校正保留体积:
| 2-乙基蒽醌 |
苯基甲基甲醇 |
| 2-甲基蒽醌 |
苯甲醇 |
| 蒽醌 |
3-苯基-1-丙醇 |
在此条件下,溶质和极性溶剂都相同,极性溶剂在流动相中也保持相同的W/V浓度,于是,1/V与分散用溶剂的密度d之间的关系就指示了溶质和稀释溶剂之间弥散性相互作用的程度和本质。所得结果列于表3-6,1/V'对分 散溶剂密度的关系曲线示于图3- 9。1/V'和I分 散溶剂的密度之间有着良好的相关关系,并为表3-6中对于溶质蒽醌的测定指数所确证。对极性较强的溶质测得的低指数值,是由于保留体积随分散溶剂密度的变化几乎可以忽脐,实际上处于测量的重现性范围以内。然而,从图3-9看出
得到的是一条直线,但对密度轴是平行的,表示与不同的烃类溶剂没有明显的弥散性相互作用。蒽醌型的溶质经常被用于证明现时可利用的所谓非极性键合相的弥散选择性,提出这点颇为重聚。一般共同接受的观点认为,弥散性相互作用比极性相互作用微弱得多,因此,要使弥散的相互作用明显地影响一个溶质的保留特性,必须使极性的相互作用非常小,至少也与弥散的相互作川处于相同的量级。这可能是前面提及的一个例子,即固定相和流动相双方对溶质的作用力都比较弱,因而弥散性相互作用的变化可对溶质的保留具有深刻影响。极性较强的溶质由于在两相中均被强烈保留,显示很小的或全然没有弥散性相互作用,所以其保留值很少随分散介质的密度而变化。当极性作用力很弱,同时可以发挥弥散作用力时,分散介质密度的变化就可能使得一系列溶质的洗脱顺序发生深刻的变化。这方面的一个例子示于图3-10。分散溶剂从戊烷转变到癸烷能使峰的洗脱顺序发生重排。图3-10中每个色谱图的第-一个峰是生育酚乙酸乙酯,第二个是乙酸苄酯,第三个是蒽醌,小峰是杂质。可以看到分辨率和洗脱顺序的显著变化几乎全由蒽醌(第三个主要峰)的移动所引起,但对分辨率的影响却十分引人注目。
为了确定常数Fa的性质,还必须做更多的工作,但自前阶段可清楚地指出,使用不同密度的分散介质是很有效的,尤其当溶质与两个相的极性相互作用较弱,而弥散力虽然也弱,却仍然可对溶质的保留作用施加显著的影响时。给出的结果说明了1/V'
与分散溶剂的密度d之间的相互关系。但应指出,同系物的烃类溶剂的密度同时与其分子量和碳原子数相关联,并在较低程度上与每毫升溶剂的极化度有关,因此,分散介质与弥散性相互作用相关的精确特性,现阶段应该是个留待讨论的问题。但从实用的观点出发,对于同系的烃类系列,可用密度作为控制弥散性相互作用的有效制数,直至发现其它参数更为合理时为止。

![硝酸铜标准溶液 c[Cu(NO3)2]= 0.01000 mol/L价格](images/202207/thumb_img/1653_thumb_G_1658537651764.jpg)








.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)