化学反应总是伴随着能量的变化(△H、△G)。依照利用途径的不同,化学反应释放的能量可以转变为不同的能量形式。25℃时,天然气与氧的完全氧化反应为
CH4(g)+2O2(g)=CO2(g)+2H2O(l)
△Hθ=-890.8kJ/mol,△Gθ=-818.4kJ/mol
燃气炉灶是用天然气与空气中的氧气燃烧,释放的热量用于加热,将化学能转化为热能;汽车发动机是先把化学能转化为热能,再通过产生高压蒸汽推动活塞产生动能;而火力发电厂则是将动能进一步转化为电能。由于燃烧反应是快速反应,所以燃烧产生的大量热传给了环境。而且每一转化过程都有一定的效率,转化的步骤越多,总的效率越低。内燃机的效率一般不超过20%。
若把化学能直接转变为电能,效率就高得多。研究化学能与电能之间转化规律的科学称为电化学。使化学能直接转变为电能的装置称为原电池。
任何自发的氧化还原反应均为电子从还原剂转移到氧化剂的过程。把锌放在硫酸铜溶液中,锌溶解而铜析出
Zn(s)+CuSO4 (aq)=Cu(s)+ZnSO4 (aq)
反应的实质是Zn原子失去电子,被氧化成Zn2+;Cu2+得到电子,被还原成Cu原子。由于锌和硫酸铜溶液直接接触,电子就从Zn原子直接转移给Cu2+,因而得不到序的电子流。随着氧化还原反应的进行,溶液温度将升高,即反应中放出的化学能转变为热能。
在图3-2装置中,氧化和还原反应分别在两个烧杯中进行。在一个烧杯中放入ZnSO4溶液和锌片,在另一个烧杯中放入CuSO4溶液和铜片,用盐桥(饱和KCl溶液的琼脂胶冻)将两个烧杯中的溶液联系起来。当接通外电路时,有电流通过。
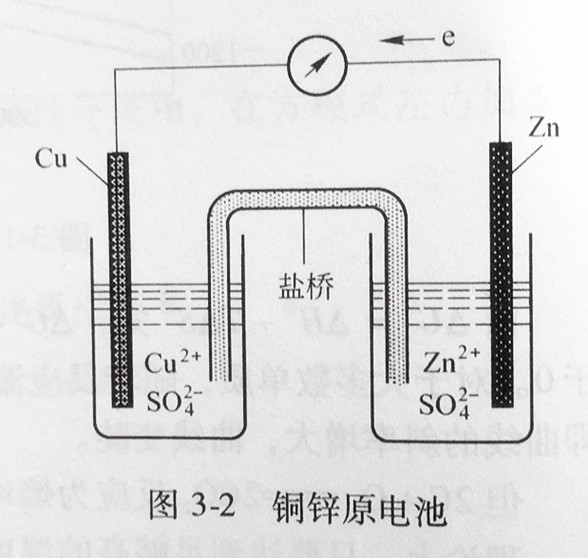
理论上,任何一个自发进行的氧化还原反应都可以组成原电池。但由于反应速率、安全性和技术条件等因素的限制,原电池可以利用的氧化还原反应仅是极少数。安全、高效的原电池一直是世界各国化学电源研究开发的热点。
原电池可用电池符号表示。书写电池符号时,习惯上把电池的负极写在左边,正极写在右边,以"│"表示相界面,以"║"表示盐桥。一般需要标明反应物质的浓度或压力。若反应物中没有电子导体,须外加惰性电极(如石墨、铂),惰性电极仅起导电作用,不参加电极反应。原电池符号的书写方式为
(-)导体│s│g│l║l│g│s│导体(+)
式中,s、g、l分别表示固体、气体和溶液。
铜锌原电池的符号为:
(-)Zn│Zn2+(c1)║Cu2+(c2)│Cu(+)
c1、c2分别为Zn2+和Cu2+的浓度。Zn和Cu既是反应物又是导体。
利用反应Cu2++H2=Cu+2H+组成的原电池的电池符号为
(-)Pt│H2(p)│H+(c1)║Cu2+(c2)│Cu(+)
铂为惰性电极,仅起导电作用,不参加电极反应。
