各种纯的液态物质,在一定外界压力下,都各有恒定的沸腾温度,此温度称为沸点。在沸点温度时,若外界供给足够的热量,液态物质可以全部气化。
纯的固态物质,又都各有其恒定的熔融温度,称为熔点,在熔点时直至固态物质完全被熔融后,温度才开始上升。
因此,测定液态物质的沸点和固态物质的熔点,是检验物质纯度的重要方法之一。但亦应该注意,某些特殊混合物其沸点也是恒定的。同样,也有些固态混合物的熔点也是恒定不变的。所以单以测定沸点和熔点的方法作唯一的检验物质纯度的标准是不确切的。有比较才能鉴别,在某些情况下要配合其他检验项目加以比较进行验证。如测定物质的比重就是其中的一个重要方法。在这里,我们将测定沸点熔点的一般方法加以介绍。
按下面图4-29将仪器装好。
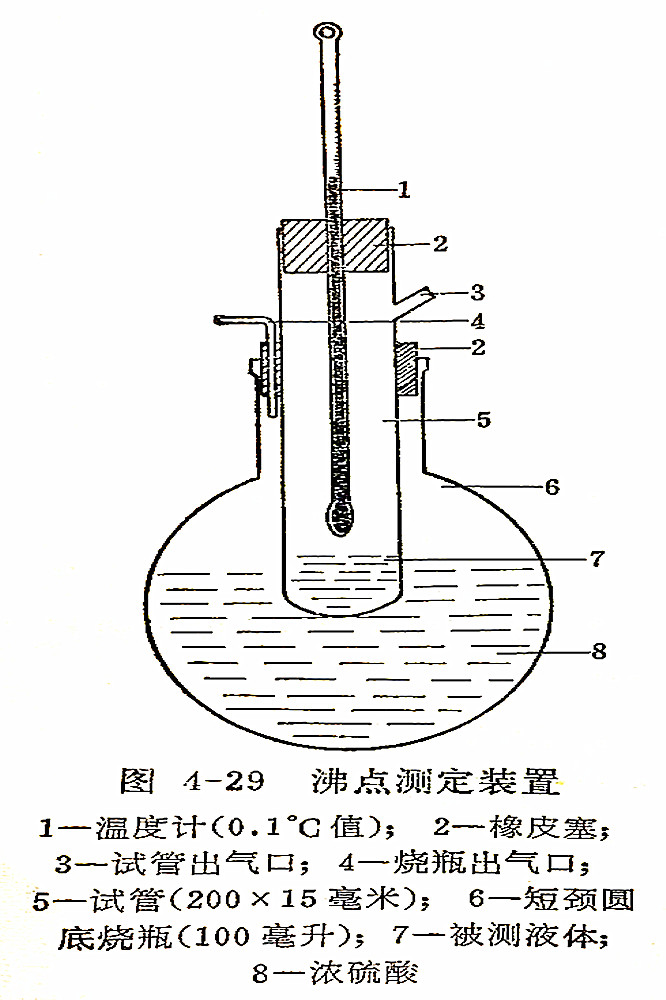
取适量的样品,注入试管中,样品的液面要稍低于烧瓶中硫酸的液面。插人试管中的温度计不要接触样品液面,温度计的下端距样品的液面约20毫米。烧瓶中的硫酸体积约为烧瓶容积的1/2。加热后,温度逐渐上升,当升到某一数值并在相当长时间内保持不变时,此时的温度即为该液体的沸点。这时样品液体在沸腾。
如果要求严格一些,测定出的温度数值还应该进行校正。要校正的计算方法有好几种,这里介绍一种不需要查阅有关换算表的计算方法。
t1=3/80(760-Pt)
t2=3/80(Pt-760)
式中 t1——当大气压小于760毫米汞柱时,观测的沸点温度应当加上的修正温度,℃;
t2——当大气压大于760亳米汞柱时,观测的沸点温度应当减去的修正温度,℃;
Pt——在实验时的大气压数值,毫米汞柱;
3/80——大气压毎变化1毫米汞柱时,其沸点的变化常数。
下面的两个图4-30,4-31都是常用的溶点测定装置。
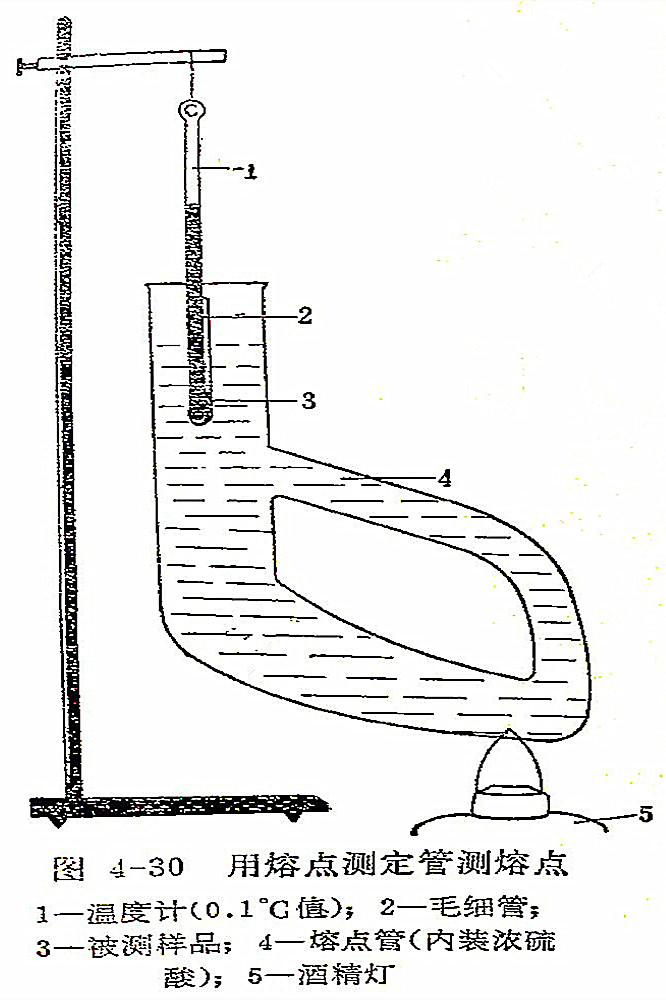
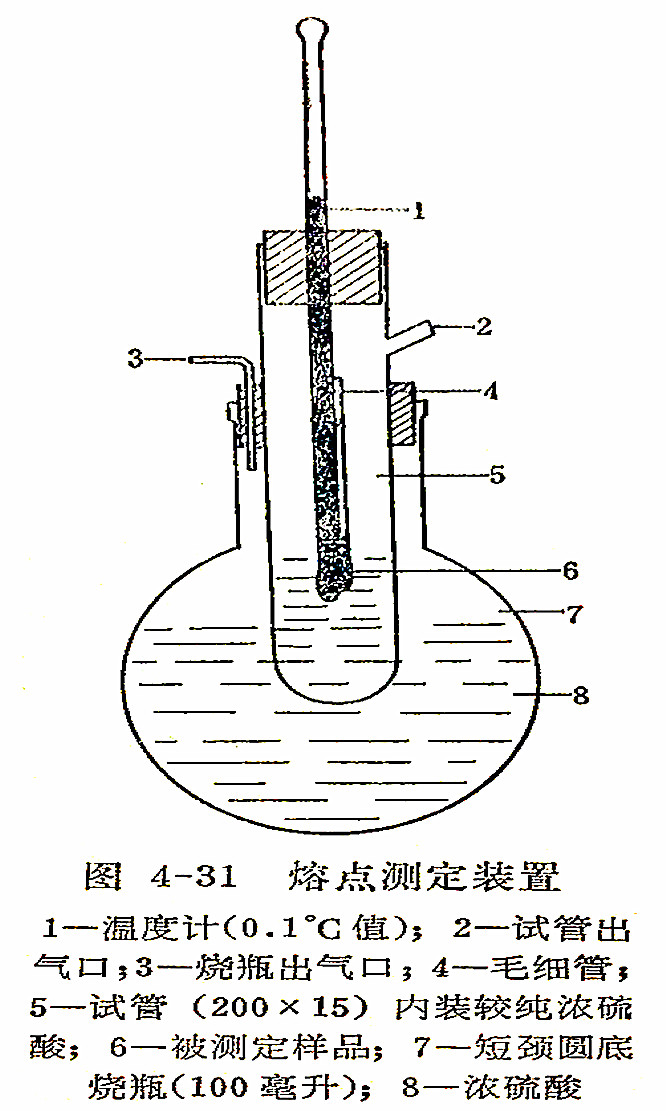
操作时,烧瓶或熔点管要特別强调洗干,不应有有机物存在。因为有机物遇浓硫酸,碳化后变黑,使观测样品的熔化情况困难。
毛细管要清洁干燥;一端封底装入样品时要在玻璃板上竖蹾几次,使样品紧缩,装入达2~3毫米高即可。样品要与温度计汞球位置水平。加热至近熔点温度前10℃时,应控制保持每分钟上升1±0.1℃的升温速度,直至样品开始熔化,记录温度为初熔温度。全熔化时的温度为全熔温度。初熔与全熔温度应在该纯物质规定以内。
如果样品易分解或易脱水,毛细管装入样品后应封闭,每分钟温度升高为3℃。
所采用的溶剂应透明清澈,而且沸点要高于样品熔点10℃以上。
