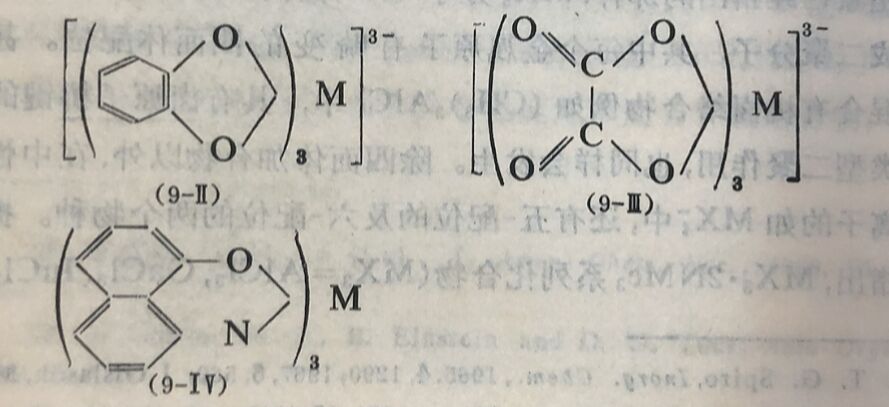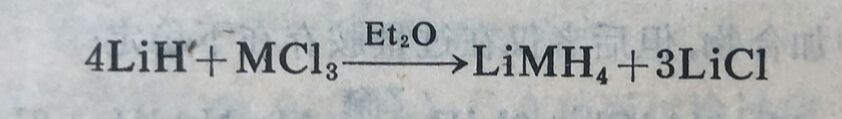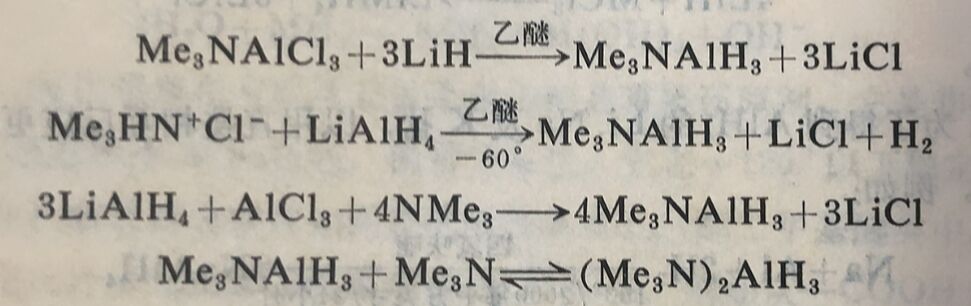人们已经注意到水合及铝酸根离子。醋酸铝的结构与Cr³⁺,Fe³⁺及其它M³⁺离子的碱式醋酸盐的相似,且可能含有碱式单元[Al₃O(OOCMe)₆(H₂O)₃]⁺,其中的水分子能解离成OH,或能被其它配位体所置换。
第III族元素最重要的八面体络合物,是那些含有蛰合环的络合物,其中典型的是β-二酮、焦儿茶酚(9-II)、二羧酸(9-III)和8-喹啉(9-IV)的络合物。中性络合物迅速地溶于有机溶剂而不溶于水。乙酰丙酮盐有低的熔点(<200°C),并且挥发而不分解。阴离子络合物,是以大的一价阳离子盐形式分离出来。8-喹啉盐用于分析目的。草酮(T)在Na[TnT₄]中生成钢的8-配位阴离子。
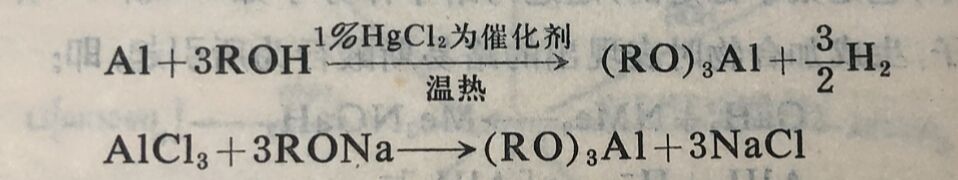
这四种元素都形成醇淦,我们可以把它们看成络合物,因为它们甚至在以情性溶剂所成的溶液中全部都是聚合的。只有铝的那些醇淦是重要的,尤其是异丙醇淦,它作为乙醛及丙酮的还原剂广泛地用于有机化学中。它们能用下列反应制得:
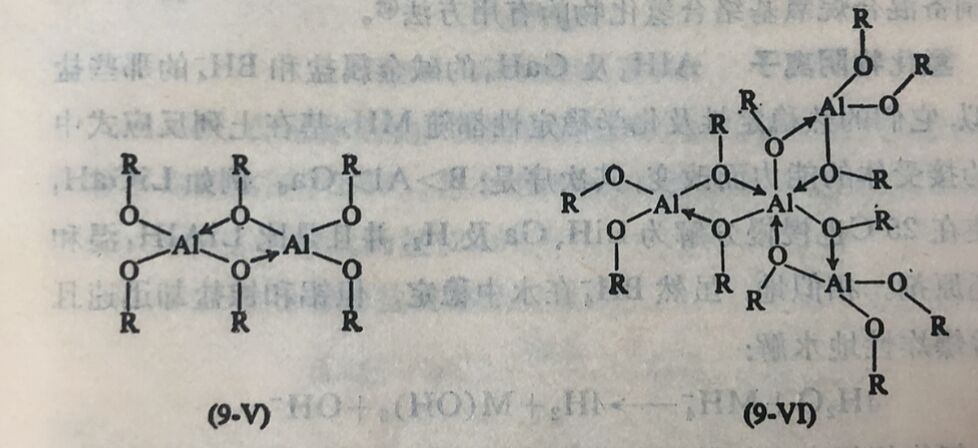
醇淦在水中剧烈水解。四丁醇淦在溶剂中是环状二聚体(9-V),而异丙醇淦在常温下是四聚的(9-VI),但在提高温度时变为三聚的。末端与桥式烷氧基可用核磁共振谱来区别。其它醇淦也能以二聚体及三聚体存在。
镓及铊分别用N₂O₅与NO₂⁺[GaCl₄]或与TINO₃、反应,形成硝酸根络合物。虽然Gaᴵᴵᴵ半径(0.62Å)仅稍小于Feᴵᴵᴵ的半径(0.64Å),但在NO₂⁺[Ga(NO₃)₄]⁻中,三价镓离子表现有单齿NO₃基,与[Fe(NO₃)₄]⁻离子不同,三价铁离子却有双齿基,并且是八-配位的。
二、络合氢化物
另外,还有一类范围广泛的络合物化学,可以把它看作是MH₃(即使分离出 简单分子,也是太不稳定的)通过与给予体分子如NR₃、PR₃、 SR₂或阴离子,生成加合物时表现出的路易斯酸行为所引起,即:
GaH₃+NMe₃→Me₃NGaH₃
AlH₃+H⁻→[AlH₄]⁻
在这样的化合物中,和硼烷衔生物有很多极相似处。AlH₃和醇类的反应:
AlH₃+nROH→(RO)nAlH₃₋n+nH₂
是制备混合烷氧基络合氢化物的有用方法。
氢化物阴离子 AlH₄⁻及GaH₄⁻的碱金属盐和BH₄⁻的那些盐相似,它们的热稳定性及化学稳定性都随MH₃基在上列反应式中 作为接受体的能力而改变,其次序是: B>Al>Ga。例如LiGaH₄即使在25°C也慢慢分解为LiH、Ga及H₂,并且是比LiAlH₄温和的还原剂。相似地,虽然BH在水中稳定,但铝和镓盐却迅速且经常爆炸性地水解:
4H₂O+MH₄⁻→4H₂+M(OH)₃+OH⁻
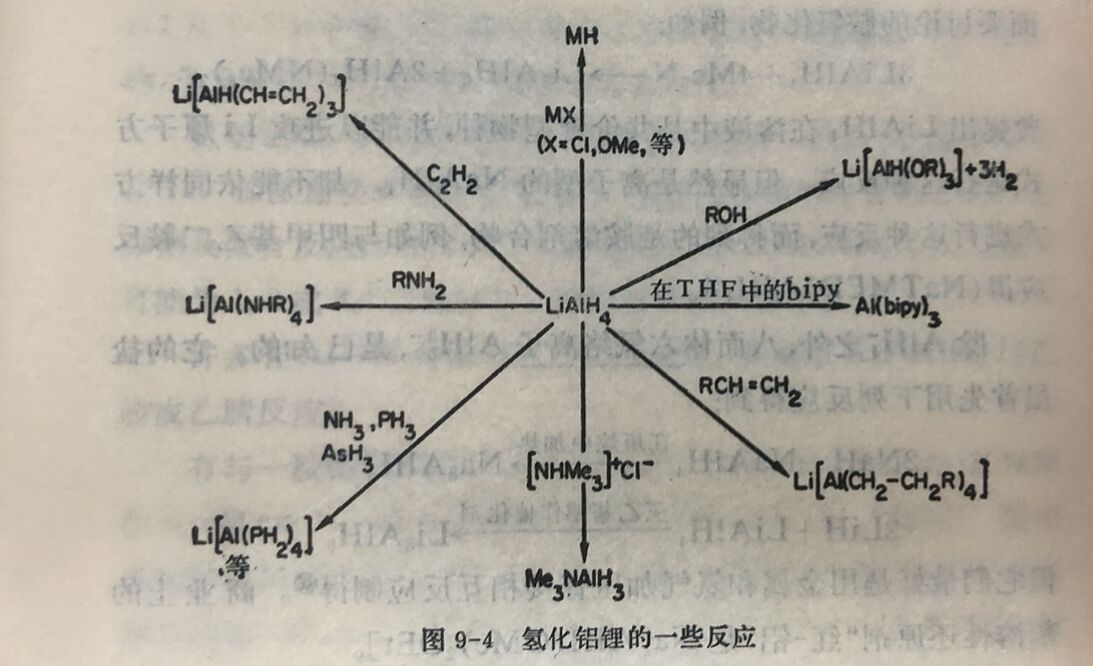
氢化铝锂在有机及无机化学中都是重要还原剂。它是非挥发性、晶态固体,纯时白色,但常为灰色。它在~120°以下稳定,且溶在乙醚及其它醚类如四氢呋哺及各种乙二醇二甲基醚类中。它 能完成许多别的冗长或困难的还原反应,例如从一COOH 到一CH₂OH。它的一些反应,表示在图9-4中。
LiAIH₄的晶体结构表明有四面体AIH₄⁻离子存在,其Al-H间平均距离等于1.55Å。每个Li⁺离子周围有四个近的氢(1.88-2.00Å)及第五个较远的氢(2.16Å)。
Al和Ga二者的盐类都能用反应:
制得。
可是,为了得到AlH₄⁻的Li,Na及K盐,以用直接相互反应更为方便。例如:
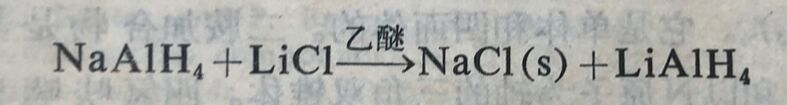
用甲苯沉淀出钠盐后,能有效地将它转变为锂盐:
虽然LiAlH₄在醚中是稳定的,但胺类溶剂能“提取"AlH₃,生成下而要讨论的胺氢化物,例如:
3LiAIH₄+4Me₃N→Li₃AlH₆+2AlH₃(NMe₃)₂
曾提出LiAlH₄在溶液中是共价键型物种,并能以进攻Li原子方式进行这种反应。但显然是离子型的NaAlH₄,却不能依同样方式进行这种反应,而得到的是胺溶剂合物,例如与四甲基乙二胺反应得(NaTMED)AIH₄。
除AIH₄⁻之外,八面体六氢络离子AlH₆³⁻,是已知的。它的盐虽首先用下列反应得到:
但它们最好是用金属和氢气加压直接相互反应制得。商业上的苯溶性还原剂“红-铝”是Na[AlH(OMe)₂OEt]。
给予体加合物 这些加合物又是和硼烷加合物类似,其稳定 性次序是: B>Al>Ga,同时也与卤化物的和烷基的加合物相类似,它们的稳定性次序是:卤化物>烷基化物>氢化物。研究最多的加合物是三烷基胺铝烷(铝烷=AlH₃)。三甲基胺生成1:1及1:2两种加合物,但后者仅在过量胺存在下稳定:
一胺加合物是白色、挥发 性、晶态固体(熔点75°),易水解,徐徐分解为(AlH₃)。它是单体和四面体的。二胺加合物是具有线状 N-AI-N和以N原子为轴的三角双锥体。四氢呋喃也可生成1:1及1:2加合物,但乙醚可能由于空间原因,只能生成1:1化合物,虽然有混合四氢呋喃-乙醚加合物存在。















































![[1,1'-双(二苯基膦)二茂铁]二氯化钯(Ⅱ)-二氯甲烷络合物](images/202401/thumb_img/5397_thumb_G_1704338141781.jpg)