碲酸
中文名称: 碲酸英文名称:orthotelluric acid别名:原碲酸、二水碲酸分子式: H6O6Te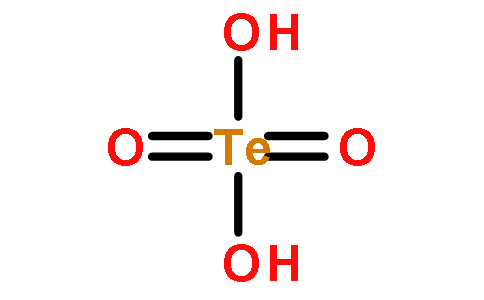 分子量: 229.64CAS号: 7803-68-1
分子量: 229.64CAS号: 7803-68-1
质检信息检验项目 指标含量, ≥98%灼烧残渣(以硫酸盐计),%≤0.002水分(H2O),% ≤0.2PSA: 121.38000LOGP: -1.44160
化学特性碲酸是一种二元弱酸,K1=6.8*10^-7 K2=4*10^-11(也有资料指出K1=1.53*10^-8,出自无机元素化学-刘新锦p134)碲酸是H6TeO6而不是H2TeO4·2H2O,碲酸的六个羟基是一样的,之所以是二元酸是因为三级电离常数小于水,无水条件下可以形成正盐(如Zn3TeO6),白色棱柱状结晶,熔点 136℃。密度 ρ(25)3.07g/mL。对光敏感。能被二氧化硫和肼等还原为元素碲,在10℃以下时与4分子水生成结晶,130℃失去2分子结晶水,加热生成三氧化碲,500℃以上生成二氧化碲。易溶于水,难溶于浓硝酸,加热100℃至200℃脱水生成中间产物(H2TeO4)n,最后完全转变为酸酐TeO3。是一种和碳酸酸性相近的弱酸,不溶于乙醇。
产品用途碲酸用作分析试剂,定量分析中分离溴化物及氯化物。可用于制取其他碲酸及碲酸盐以及用作氧化剂。用强氧化剂将碲氧化为碲酸。
生产方法由硫酸与碲酸钡作用或用强氧化剂氧化单质碲制得1.将理论量的无水碳酸钾(纯级)、水和少量30%的过氧化氢(纯级)加到研细的试剂二氧化碲中,不断搅拌并加热至105-110 oC,保温30min,[Teo2+H2O2+K2co3=K2TeO4+CO2↑+H2O]当气泡不再溢出时,冷却混合物,滤去不溶物,滤液用水稀释,然后分次少量加入KY-2(H-型)阳离子交换树脂。控制混合物的PH<3,滤出树脂并应水洗涤树脂数次,洗液并入滤液,将该溶液以一定速度通过填有KY-2(H-型)洗涤交换柱,合并洗液及溶液,加热蒸发至出现结晶薄膜,冷却,加入溶液体积两倍的95%乙醇,静置后过滤,结晶用95%乙醇洗涤后,于真空下干燥,即为成品。2.将13g碲粉装入带在回流冷凝管的圆底烧瓶中,用5mL 50%的硝酸将其完全湿透。将反应装置置于通风橱中,分次加入150mL 10%的氯酸溶液,可加热使反应激烈发生,此时溶液应处于沸腾状态,并有大量氯气生成,加热回流30min,使碲完全溶解。先用直火加热蒸发溶液,然后在水浴上蒸发至有结晶出现,在搅拌下用冰水浴冷却结晶,即可析出微细的白色结晶。将结晶滤出后用热水溶解并重结晶一次。用玻璃砂芯漏斗吸滤,先用少量的冰水,后用乙醇和乙醚洗涤,最后在放有P2O5的真空干燥器干燥。3.将10g TeO2在40mL浓硝酸和100mL水中的悬浮液加热至沸,并在猛烈搅拌下分次慢慢加入100mL 5%的高锰酸钾溶液,每隔5min加入5mL,然后搅拌和煮沸。当全部高锰酸钾溶液加完后,使溶液在沸腾温度下保持50min,这样可减少MnO2生成的量。然后慢慢地加入3%的H2O2溶液,直至MnO2全部溶解,成为澄清的溶液。将此溶液蒸发到约剩60g时加入10mL浓硝酸,静置24h可析出原碲酸结晶。将母液倾出,蒸发至约25g时再用10mL浓硝酸进行同样的处理,又可得到部分结晶。将两次所得的结晶合并后用浓硝酸洗涤三次,每次用10mL硝酸,且每次洗涤后要尽量将晶体弄干。然后将晶体用25mL水和17mL浓硝酸组成的溶液重结晶一次,再用蒸馏水重结晶一次。最后将结晶用少量冰水、乙醇和乙醚依次洗涤,并在放有P2O5的真空干燥器中干燥。
产品信息 [颜色] 白色 [重量] 25g 危险性类别 [危险性类别] 非危化品
