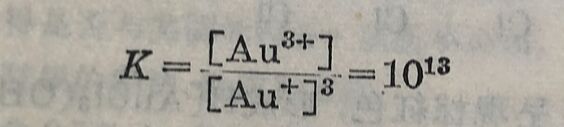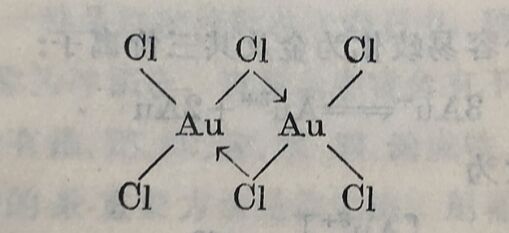金
铜臭 / 2022-08-03
一、金的存在和冶炼
由于金非常不活潑,故多以自由状态的自然金存在于自然界。自然金有两种,一种是以微粒散布于岩石中,称岩脉金,另一种是存在于砂礫中,称为冲积金。自然金中常含有不同量的銀(最高达50%),有时还含有鉑、鈀、銠、鉍、汞銅、鉛或铁。
提取自然金的最重要方法是氰化法。用稀(約0.03-0.2%)NaCN溶液处理被粉碎了的矿石,然后通入空气使金粒溶解,再用鋅自溶液中将金置换出来:
4Au+8NaCN+2H₂O+O₂=4Na[Au(CN)₂]+4NaOH
2Na[Au(CN)₂]+Zn=Na₂[Zn(CN)₄]+2Au↓
二、金的性质和用途
金呈黄色,有光澤,比銀軟,延性高,可以拉成5x10⁻⁴克/米的絲,展性也高,可以碾成1x10⁻⁵毫米厚的箔。金可与鉑、鈀、銀或銅形成合金,比純金硬,但熔点較低。
金的化学活性比銅和銀皆低,在空气中和水中皆无变化。与卤素只在高温下才发生作用,不与硫直接化合。金不溶于一般的氧化性酸中,只溶于王水中:
Au+4HCl+HNO₃=HAuCl₄+NO+2H₂O
由上式可見,在王水中使金溶解的氧化剂仍然是硝酸,而不是产生了有更高氧化能力的其它化合物,但纯确酸不能存在就发生作用,这是因为后者的氯离子与金络合,形成[AuCl₄]⁻络离子,从而降低金的氧化电位,
Au=Au³⁺+3Θ E⁰=+1.50 伏
Au+4Cl⁻=[AuCl₄]⁻+3Θ E⁰=+100伏
这就使金容易氧化得多。
金常用于电镀,制作化学器皿和装饰品。“紅宝石玻璃”中含有胶态的金屬金。
金的一价离子容易歧化为金及其三价离子:
3Au⁺⇔Au³⁺+2Au
这反应的平衡常数为
故一价金屬离子不能在水溶液中存在,即使是溶解度很小的 AuCl都在水中分解。但格离子如[Au(CN)₂]⁻, [Au(S₂O₃)₂]³⁻,[Au(SO₃)₂]³⁻里的一价金却很稳定。
金的三价离子为棕色,络合傾向很大,如氯化金溶于水即变为络阴离子:
AuCl₃+H₂O=H[AuCl₃(OH)]
此外还有[AuCl₄]⁻, [Au(CN)₄]⁻等。这些格离子的结构都呈平面四方形,配位电子在dsp²杂化軌道。
(i)氧化物和氫氧化物将三氯化金的溶液用氫氧化鈉处理,得到黄棕色的氢氧化金Au(OH)₃沉淀。用五氧化二磷使它脱水,得到棕色的AuO·OH粉末,在140°下长时周加热,可形成棕色的氧化金Au₂O₃;如温度稍高,即分解为Au₂O。
氩氧化金⁽ᴵᴵᴵ⁾具有两性,酸性較强,故称为金酸。它溶解于碱中形成金酸盐,自盐溶液中析出的有淡黄色的K[AuO₂]·3H₂O和绿色的Ba(AuO₂)₂·5H₂O。
(ii)卤化物 氟化金⁽ᴵᴵᴵ⁾可用金与三氟化溴作用而制得。这两者反应生成秸晶盐AuBrFe₆,加热即分解为氟化金AuF₃,在500°以下稳定。氯化金⁽ᴵᴵᴵ⁾和溴化金⁽ᴵᴵᴵ⁾可由金和卤素直接作用而制得。适量的三氯化金与碘化鉀在溶液中作用,生成碘化金⁽ᴵᴵᴵ⁾。
无水氯化金AuCl₃可由金与氯在200°直接作用而制得。AuCl₃是紅色晶体,在180°C以上有显著的揮发性,在气态中以双聚物Au₂Cl₆形式存在:
AuCl₃易溶于水,呈現棕红色,形成H[AuCl₃(OH)]。如果加入盐酸,溶液即变为檸檬黃色,而形成氯金酸:
H[AuCl₃(OH)]+HCl=H[AuCl₄]+H₂O
将金溶于王水中,蒸发以除去盐酸,即有黄色的針状晶体析出,为四水合氯金酸。若用酒精作溶剂,則析出的秸晶是无水氯 金酸。常見的氯金酸盐有黄色的K[AuCl₄]·2H₂O和Na[AuCl₄]·2H₂O。氯金酸銫溶解度很小,有时利用来鉴定金元素。
(iii)氰化物 在氯化金⁽ᴵᴵᴵ⁾溶液中加氰化鉀,蒸发溶液,可結出四氰金甲酸鉀的水合物K[Au(CN)₄]·3/2H₂O,为无色片状晶体,溶解度很大。水合物加热至200°时,即脱水变为无水盐。