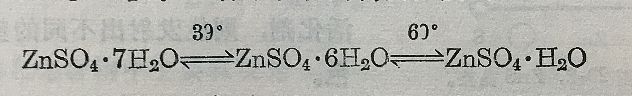鋅的化合物
铜臭 / 2022-08-03
鋅在化合物中只表现为+2价。离子呈无色,只要阴离子星无色,则所形成的鋅盐都是白色。除氟化物外,其他的卤化物、硫酸盐、硝酸盐和酷酸盐都易溶于水。氧化卸、氧氧化鋅、硫化鋅、碳酸鋅等皆微溶于水。锌离子形成絡合物的倾向小于銅离子。
1.氧化鋅和氫氧化鋅
鋅在空气中燃燒产生氧化鋅ZnO,大量制造可用此法。在实驗室内,把碳酸鋅加热分解即可制得氧化鋅。
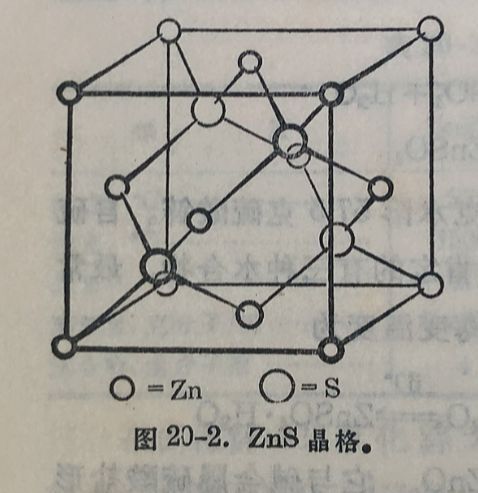
純氧化鋅为白色,加热则变为黄色,晶格屬ZnS类型(見图20-2)。由晶格类型和Zn-O鍵长等性质可知,氧化鋅是共价化合物。它在水中只微溶,溶度积为1.8×10⁻¹⁴(20°C)。溶于不同的酸而得各种鋅盐。它用作白色塗料,虽然“附着力”不如鉛白,但它遇到硫化氢时顏色不变。在合成甲醇时,氧化鋅可用作催化剂。它也是橡胶的填料。
氢氧化鋅可用間接方法制取,即在鋅盐的溶液中,加入适量的强碱,即析出白色氫氧化鋅。氫氧化鋅是两性化合物,在飽和溶液中有下列平衡存在:
Zn⁺⁺+2OH⁻⇔Zn(OH)₂⇔H⁺+HZnO₂⁻
溶于强碱而形成鋅酸盐:
Zn(OH)₂+2NaOH=Na₂[Zn(OH)₄]
溶于酸中形成鋅盐:
Zn(OH)₂+2H⁺=Zn⁺⁺+2H₂O
前已述及,氫氧化鋅也溶于氨水中,形成氨絡离子。
2.卤化锌
将氧化锌或碳發斜容解于氢卤酸中而制得卤化算。除Znl₂呈黄色界,其他都是白色晶体在空气中都吸水而潮解。
从表20-3可知,卤化物中,氟化鋅的熔点和沸点最高而且不落于水。其余卤化鋅都溶于水,自溶液中析出水合物。它們与碱金量的卤化物形式复盐。通式为M⁽ᴵ⁾ZnX₃、M₂⁽ᴵ⁾ZnX₄与M₃⁽ᴵ⁾ZnX₅。
表20-3 卤化锌的性质
|
性质
|
ZnF₂
|
ZnCl₂
|
ZnBr₂
|
ZnI₂
|
|
熔点,°C
沸点,°C
比重
溶解度,克分子/升
水合物,水分子数
|
872
1500
4.8
5×10⁻⁵
4 |
262
732
2.9
27
4、3、2.5、1.5、1
|
394
650
4.2
21
3、2
|
446
624
4.7
14
4、2
|
在卤化鋅中以氯化鋅为最重要。水合氯化鋅ZnCl₂·H₂O与 MgCl₂·6H₂O, BeCl₂·4H₂O一样在加热时不易完全脱水,而是形成碱式盐:
ZnCl₂·H₂O⇔Zn(OH)CI+HCl
ZnCl₂是固体中溶解度最大的一个。在10° 时每100克水溶330克无水盐。在它的浪溶液中可形成格合酸(与AuCl₃同),此酸有显著的酸性:
ZnCl₂+H₂O=H[ZnCl₂(OH)]
因此,它能溶解金屬氧化物,如氧化铁⁽ᴵᴵ⁾:
FeO+2H[ZnCl₂OH]=H₂O+Fe[ZnCl₂OH]₂
在焊接金属时,用ZnCl₂溶液清除金屬表面上的氧化物就是根据上述的性质。
ZnCl₂和ZnO的混合水溶液能迅速硬化,生成Zn(OH)Cl,是牙科中常用的粘合剂。大量的氯化錦用于印染上和染料的制备上。氯化鋅的吸水性很强,故在有机综合上用做去水剂。浸过ZnCl₂溶液后的木材不易被腐仙。浸过ZnCl₂溶液可溶解微摊素,因此常用于制造牛皮紙。
3.硫酸鋅
将氧化鋅溶解于稀硫酸中,或在700°下焙燒硫化鋅,均可得到硫酸鋅:
ZnO+H₂SO₄=ZnSO₄+H₂O
ZnS+2O₂=ZnSO₄
它易溶于水,在25°C时,每100克水溶57.5克硫酸鋅。自硫酸鋅溶液中可析出它的水合物。已經肯定的有三种水合物,最常見的是ZnSO₄·7H₂O。三种水合物的轉变温度为
无水盐加热到770°即分解为SO₃和ZnO。它与碱金屬硫酸盐形 成复盐M₂⁽ᴵ⁾SO₄·ZnSO₄·6H₂O。
硫酸鋅用于印染上,在镀鋅时作为电解质,在医药上用作收斂剂。
4.硫化鋅
自然界存在的ZnS称为閃鋅矿。在鋅盐溶液中加入(NH₄)₂S,析出的白色沉淀就是碗化鋅ZnS:
Zn⁺⁺+(NH₄)₂S=ZnS+2NH₄⁺
硫化鋅在酸性溶液中不能沉淀出来,在中性溶液中涵以H₂S也不能使它完全沉淀,因为在反应的过程中H⁺离子濃度增加,阻碍ZnS进一步沉淀:
Zn⁺⁺+H₂S=ZnS+2H⁺
如果使溶液变为碱性,再通以H₂S,則ZnS可沉淀完全:
HZnO₂⁻+H₂S=ZnS+OH⁻+H₂O
硫化鋅在水中的溶解度很小,溶度积为1.2x10⁻²³(18°C)。溶于HCI,但不溶于醋酸中,因为后者的氨离子濃度很小,虽然形成HS⁻,但溶液中S⁻⁻离子的濃度仍然能使[Zn⁺⁺][S⁻⁻]> 1.2x10⁻²³。
硫化鋅在硫化氩气流中灼燒,轉化为晶体,其秸构如图20-2所示,S居于Zn所构成的四面体中,Zn也在S的四面体中,配位数皆为4,是一种典型的晶格。如晶体硫化鋅含有微量的銅或銀的化合物做为活化剂,則能发射出不同的螢光顏色。






































![硝酸铜标准溶液 c[Cu(NO3)2]= 0.01000 mol/L价格](images/202207/thumb_img/1653_thumb_G_1658537651764.jpg)