





































今天我们将研究铁的氧化物、氢氧化物、铁的盐类以及铁盐的检验。
在上一偏文章里我们已经知道,铁眼别的物质起反应通常会失去2个或3个电子,因此,铁能形成+2价和+3价的两类化合物.下面所研究的铁的氧化物、氢氧化物和盐类中,各都有+2价和+3价的两类化合物。
铁的氧化物 铁的氧化物有氧化亚铁、氧化铁、四氧化三铁三种.铁在空气里灼热或在氧气里燃烧时,都有黑色的氧
化亚铁(FeO)伴同红色的氧化铁(Fe23)生成:
氧化亚铁跟氧化铁会结合生成暗褐色的四氧化三铁(Fe3O4)在锤击赤热的铁时,生成的“铁渣”就是Fe3O4,赤热的铁跟
水蒸气反应时,也生成Fe304.
氧化铁在高温下眼氢气或一氧化碳反应,会生成氧化亚铁:
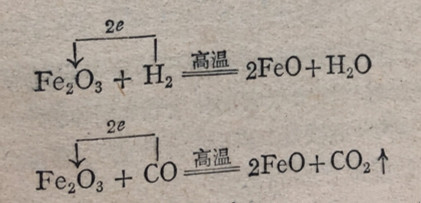
铁的氧化物都不溶于水,和水不发生反应,但它们都是碱性氧化物,能跟酸起反应生成盐.例如
Feo+H2S04 =Feso4+H2O
Fe2O3+6HCI= 2FEC13+ 3H20
铁的氢氧化物 与氧化亚铁和氧化铁相对应的碱是氢氧化亚铁[Fe(OH)2]和氢氧化铁[Fe(OmH)],这二种氢氧化物都可用相应的可溶性铁盐跟碱溶液反应而制得.如亚铁盐(即+2价的铁盐)溶液跟碱溶液起反应,就生成氢氧化亚铁的沉淀.例如:
Feso4+2NAOH=Fe(OH)2↓+Na2s04
用简化离子方程式表示:
Fe+++20h-=Fe(OH)2↓
氢氧化亚铁是絮状的白色沉淀,在空气里很快地被氧化,先变成淡蓝色,再变成淡绿色,最后变成红褐色的氢氧化铁:
4FE(OH)2+O2+2H20= 4FE(OH)3
铁盐(即+3价的铁盐)溶液跟碱溶液起反应,就生成氢氧化铁的絮状红褐色沉淀.例如:
Fecl3+3NAOH= Fe(OH)3 ↓+3NAC1
用简化离子方程式表示:
Fe+++十+3OH-=Fe(OH)3↓
氢氧化铁受熱,会失水而生成红色的氧化铁粉末:
2FE(OH)3=加热=FE2O3+3H2O
氢氧化亚铁和氢氧化铁都是不溶于水的碱。
铁的盐类 铁由于它的化合价的不同而生成两种盐类:+2价铁盐类(亚铁盐)和+3价铁盐类(铁盐).较重要的铁的盐类有硫酸亚铁和氯化铁。
1.硫酸亚鉄(FeSO4)通常所见的绿矾,就是含有7个结晶水的硫酸亚铁晶体(FeSO4・7H20),呈浅绿色,很易溶解于水.在空气里,硫酸亚铁晶体易失去结晶水,同时氧化成黄褐色的硫酸铁[Fe2(SO4)3]。
硫酸亚铁可用铁屑跟稀硫酸反应而制得:
Fe+H2SO4(稀)=FeSO4+H2个↑
硫酸亚铁可用来杀灭农作物害虫,在工业上,用来制造某些颜料,墨水以及在织物染色时用作媒染剂等。
2.氯化铁(FeCl3)氯化铁是棕黑色固体,常见的是含有6个结晶水的深黄色固体,容易潮解。
氯化铁溶液遇些还原剂(如H2,Fe等)》能被还原生成化亚铁:
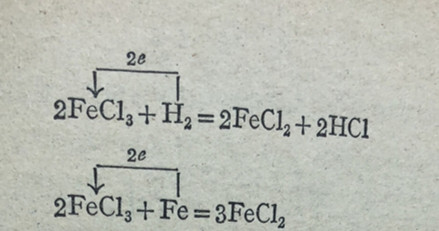
氯化铁可用氧化铁眼盐酸反应或由氯化亚铁眼氯气反应而制得:
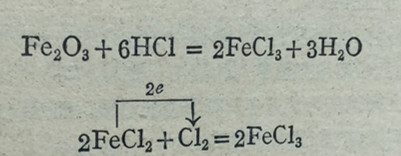
氯化铁在医药上用作止血剂,在染料工业上用作氧化剂。
从氯化铁的性质和制法中我们看到,氯化铁在某些还原剂的作用下可以变成氯化亚铁;氯化亚铁在某些氧化剂的作用下可以变成氯化铁,这一事实说明了+2价铁和+3价铁在一定的条件下是可以相互转化的:

铁盐的检验 验我们可以利用无色的硫氯化钾(KCNS)的溶液来检验可溶性铁盐(也就是检验Fet+t).在铁盐溶液里
滴入几滴硫氰化钾的溶液,铁盐溶液立刻变成深红色,这是由于生成深红色的硫氰化铁[Fe(CNS)3]的缘故.这个反应的的
化学方程式是:
Fecl3+3KCNS=Fe(CNS)3+3KC1
简化离子方程式是:
Fe+++SCNS-=Fe(CNS)3
亚铁盐遇硫氯化钾溶液不显红色。
