稳定同位素的分离
铜臭 / 2022-08-11
稳定同位素的分离,有着重大的意义,因为有些是在原子能利用中作为原材料的,如重水、重氫、Li⁶ ⁷又如U²³⁵虽然是一个放射性同位素,但是他的牛衰期是那末长(8亿年),它的制备原理是和稳定同位素样的,所以也作为稳定同位素看待,而在本节中叙述。其次,稳定同位素广泛应用来作为标記原子,除重氢外,如N¹⁵和O¹⁸由于沒有寿命够长的放射性同位素,因而非用它們本身不可。其他还用到C¹³,Cl³⁵等等。
分离同位素的原理有: (1)利用质量的不同,可用电磁分离法、 扩散法、离心扩散法; (2)利用同位素分子的不同热力学性质,可用 同位素交换法、精餾法; (3)利用不同的动力学性质,可用电解法; 等停。
1.精餾
含有不同同位素的分子,例如H₂和HD, H₂O和HDO(半重水),H₂O 和H₂O¹⁸(重氧水),有着不同的蒸气压,其比值列于表27-5中。
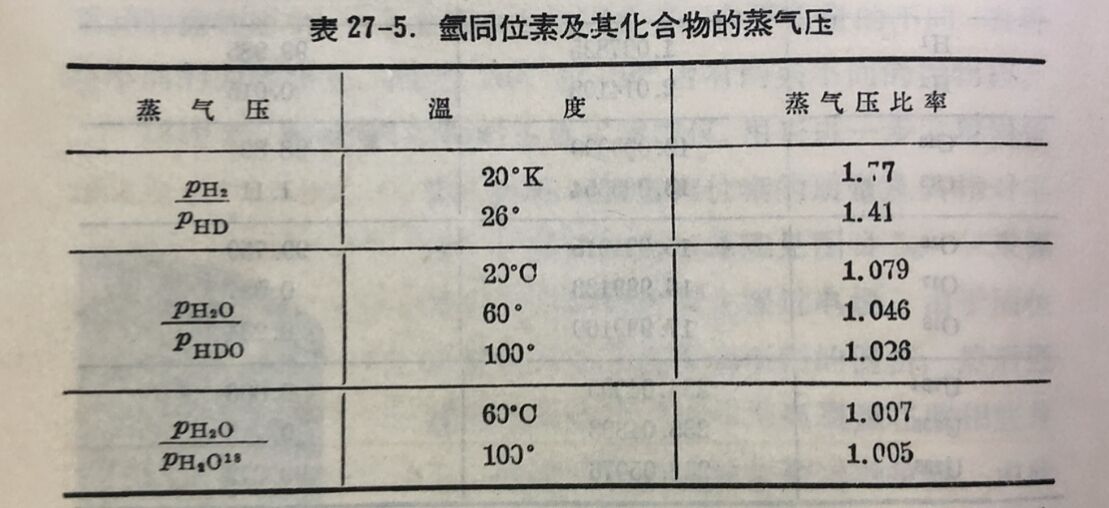
由此可見,在較低溫度时进行蒸餾比較有利。溫度过低时,蒸气压本身太小,而使精馏效率很低。在欲富集HDO和H₂O¹⁸时,一般調节至60°C。但是,一次蒸餾的结果,所得富集程度是很小的。蒸气压比率就是分离系数。所以必须进行分級蒸佩,或称精餾。举例說,天然水中含HDO达0.03克分子百分数,若蒸餾100次,实际上是使用100个塔板的精餾柱,秸果可以富集到
0.0003×1.046¹⁰⁰=0.0269
即制得2.69克分子百分数渡度的HDO。在重水D₂O制造的方法中,用精餾法处理大量的水时,消耗能最太大,故常用来对已经初步富集的重水作最后富集。
对富集氧同位素来說,精餾是最好的方法。天然水中含0.20克分子百分数H₂O¹⁸,用100塔板的精餾柱,可以富集到
0.002x1.007¹⁰⁰=0.004
即得0.40克分子百分数H₂O¹⁸。这个演度,已可作为标记原子之用了。若重复精你,或使用更多的塔板(可用翱小的不锈钢缺六棱环为增料),可将渡度再行提高。但当滇度較高时,就不能用上列簡单式叶算(重水亦热)。结果如下:
| 塔板数(蒸馏次数) |
500 |
1000 |
1500 |
| 富集程度,克分子百分数 |
6.55 |
68.2 |
98.6 |
约在20°K低温进行液氨精幅,是制造重氢的主要方法之-。虽然用此法富集重氫一般至4%D₂,然应指出,在重水生产中,从0.015%富集到 1-2%,由于处理大量物料之故,其费用要占全部成本的90%。
2.同位素交换法
含有不同同位案的同种分子,例如H₂O和HDO,有着不同的反应性能,因此有所謂“同位素平衡”,例如
H₂O(气)+HD(气)=HD0(气)+H₂(气)
表27-6 氢与水间同位交换的平衡常数
| 温度°C |
平衡常数K |
温度°C |
平衡常数°C |
|
0
25
50
|
4.17
3.62
3.20
|
75
100
125
|
2.88
2.62
2.42
|
但是这一反应的速度非常缓慢,甚至到不能察觉的地步。要用鉑或較有效的Ni-Cr₂O₃接触剂(Ni:Cr原子比率=85:15),在60-75°时进行交换。D富集在水分子中。
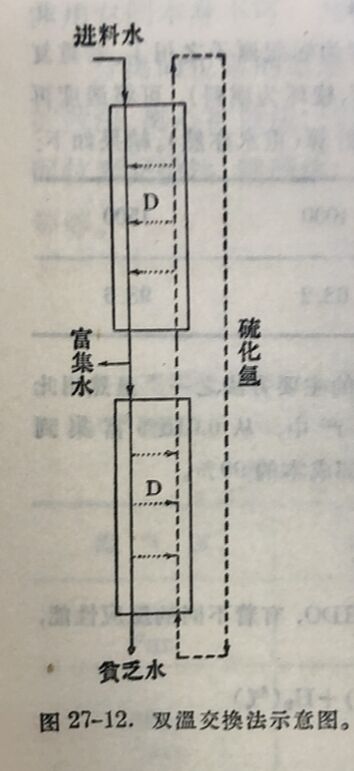
利用不同温度下的不同分离系数来富集同位案,这叫做双温交换法。例 如H₂O(液)+HDS(气)⇔HDO(液)+H₂S(气)的平衡常数,在30°为2.22;在130°为1.76。用图27-12所示的装置,在20大气压下,把硫化氩作为循环气体,由下向上通过热塔时不断由水中提取D,而在通过冷塔时不断把D送还到水中。同时,向下迎流的水在通过洽塔后,水中的重水濃度不断增大,可在治塔底引出一小部水(富集水)作为产品,当水继糠流下热塔时,核出D后即作为威水(贫乏水)流出。使用一个合适的两般装置,可把天然水富集到15% D₂O,然后接用精储法提濃到99.8% D₂O。本方法不受产量的限制,适用于大规模制造重水。
同位素交换法也用来分离鋰同位素Li⁶和Li⁷。使鋰汞齐和鋰化合物溶液間进行交换,Li⁶富集在汞齐中,分离系数約为1.05。